- 작성자오대균
- 작성일시2021.01.22 17:06
- 조회수7,642
바이오의약품 후보물질 개발 전략 수립 지원
1. 바이오의약품 최적화 전략 수립 시 고려사항
바이오의약품의 개발은 높은 비용과 오랜 기간이 소요되므로 개발과정 초기에 제품화 요건, 인허가 요건 및 사업적 경쟁력을 철저하게 고려해야 한다. 또한 개발을
실패하거나 개발과정을 재시행할 경우 막대한 손실이 발생하게 되므로 철저한 계획 수립과 마일스톤 관리가 반드시 요구된다.
2. 바이오의약품 제품 설계와 이를 기반한 개발 과정 수립
○ 사업적 가치를 극대화하기 위해서는 우선 시판 또는 개발 중인 의약품에 대한 철저한 비교 분석이 수행되며, 경쟁력 있는 목표 제품 사항(Target Product Profile) 및
품질 목표 제품 사항(Quality Target Product Profile) 설정과 특허 전략 수립이 진행된다.
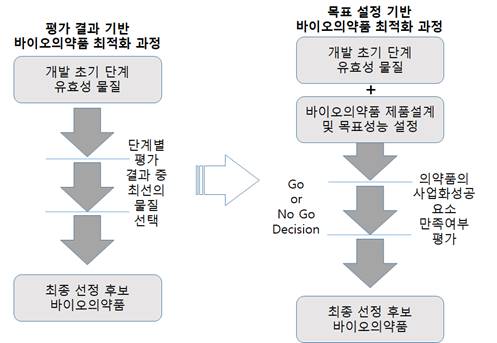
○ 바이오의약품 최적화 계획 수립은 목표 제품 사항과 품질 목표 제품사항이 확보될 수 있도록 개발 단계별 구체적인 목표를 포함하여 설계되어야 한다. 초기물질
발굴 후 최적화 과정을 아래 그림 왼쪽의 개발단계와 같이 최선의 물질을 선택하는 방식으로 진행할 경우 상업화 요구조건이 부족한 후보물질이 최종 도출되는
경우가 발생될 수 있기 때문이다. 따라서, 마일스톤 각 단계별 목표를 설정하고, 이를 기반하여 진행여부를 결정하는 개발이 이루어져야 한다.
<그림 1. 목표 제품 프로파일 설정 기반 바이오의약품 최적화 과정>
3. 신약개발지원센터 신약개발최적화지원부의 바이오의약품 최적화, 인허가 및 제품화 전략 지원
○ 경쟁 의약품 비교 및 기술동향 분석 제공
의약품 시장은 질환별, 치료단계별, 진단결과별 다양한 요건에 따라 세분화하여 평가된다. 신약개발지원센터 신약개발최적화지원부에서는 세분화 된 영역에
포함된경쟁의약품의 약효, 안전성, 안정성, 생산성, 적용된 플랫폼 기술 등 상세 분석을 통해 개발 중인 의약품이 상업적 경쟁력이 확보되도록 개발자를 지원
하고 있다.
○ 경쟁력 및 인허가 요건을 고려한 TPP, QTPP 설계 지원
바이오의약품의 제품화, 사업화, 기술이전 등의 과정에서 발생할 수 있는 시행오류를 개발 시 고려하도록 제품 관리 항목 설정 및 정략적 목표 품질 수립을
지원하고 있다. 아래의 표는 FDA 가이드라인에서 제시하고 있는 항목들을 정리한 것이다.
<표 1. 목표 제품 사항 (Target Product Profile; TPP) 예시>
|
항목 |
|
|
1. 약물이름 (Product) |
|
|
2. 적응증(Clinical Indication) |
|
|
3. 제품 유형(Product Type/Format) |
|
|
4. 투여용량 및 투여 경로 (Dose and Administration) |
|
|
5. 제형(Dosage Form) |
|
|
6. 임상 및 비임상 효능(Efficacy) |
약리학적 효능 (Pharmarcological Effect) |
|
작용기전(MOA, Mode of Action) |
|
|
약력학(Pharmacodynamics) |
|
|
약동학(Pharmacokinetics) |
|
|
7. 안전성 (Safety) |
금기사항(Contraindications) |
|
경고 및 주의사항(Warnings and Precautions) |
|
|
부작용 (Adverse Reactions) |
|
|
상호작용 (Drug Interactions) |
|
표 2. 제품의 품질 목표 사항 (Target Product Profile; TPP)의 예시
|
항목 |
|
1. Dosage Form |
|
2. Protein Content per vial |
|
3. Dose |
|
4. Concentration |
|
5. Mode of Administration |
|
6. Viscosity |
|
7. Container |
|
8. Shelf Life |
|
9. Complatability with Manufacturing Processes |
|
10 .Biocompatibility |
|
11. Degradants and Impurities |
|
12. Pharmacopoeial Compliance |
|
13. Aggregate |
|
14. Fucose Contents |
|
15. Galactosylation (%G1+G2) |
|
16. HCP |
|
……. |
○ 후보물질 최적화 및 특허 마일스톤 관리 전략 수립 지원
바이오의약품의 제품화, 사업화, 기술이전 과정에서 발생할 수 있는 시행착오를 줄일 수 있도록 바이오의약품 최적화 마일스톤 및 관리 전략 수립을 지원하고 있다.
* 상담 연락처: 신약개발지원센터 신약개발최적화지원부 최원석 부장 (wschoi@kbio.kr; 043-200-9510)

